您现在的位置是: 首页 > 教育政策 教育政策
江苏高考化学2017答案,江苏高考化学2017答案详解
tamoadmin 2024-05-23 人已围观
简介1.江苏省2016年小高考化学试卷2.中2013年江苏高考化学题第15题不明白,盼您详细讲解分析,谢谢! 正确答案为CD3.江苏化学高考是什么卷4.2012江苏化学高考卷15题解析CD 本题属于基本理论中化学平衡问题,主要考查学生对速率概念理解与计算,平衡常数概念与计算,平衡移动等有关内容理解和掌握程度。高三复习要让学生深刻理解一些基本概念的内涵和外延。 A.在I中充入1molCO和1molH2
1.江苏省2016年小高考化学试卷
2.中2013年江苏高考化学题第15题不明白,盼您详细讲解分析,谢谢! 正确答案为CD
3.江苏化学高考是什么卷
4.2012江苏化学高考卷15题解析
CD 本题属于基本理论中化学平衡问题,主要考查学生对速率概念理解与计算,平衡常数概念与计算,平衡移动等有关内容理解和掌握程度。高三复习要让学生深刻理解一些基本概念的内涵和外延。 A.在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,刚开始时,容器I、中正反应速率最大,容器II中正反应速率为零。达到平衡时,容器I温度大于700℃,容器II温度小于700℃,所以,容器I中正反应速率大于容器II中正反应速率。 B.容器III可看成容器I体积压缩一半,各物质浓度增加一倍,若温度恒定,则平衡不移动;但恒容绝热的情况下,容器III中温度比容器I高,更有利于平衡向逆反应方向移动,故平衡常数容器III小于容器I。 C.若温度恒定,容器I、II等效,但两者温度不等。达到平衡时,容器I温度大于700℃,容器II温度小于700℃,有利于容器I平衡向逆反应方向移动,故容器I中CO的物质的量比容器II中的多。 D.若温度恒定,容器I、II等效,容器I中CO的转化率与容器II中CO2的转化率之和等于1。但两者温度不等,达到平衡时,容器I温度大于700℃,容器II温度小于700℃,有利于容器I平衡向逆反应方向移动,有利于容器II平衡向正反应方向移动,故容器I中CO的转化率相应减小,容器II中CO2的转化率同样会相应减小
江苏省2016年小高考化学试卷
2017年江苏高考总分480分(语数外),其中选修两门按比例划分等级A+、A、B+、B、C、D,不计算分数。
普通高中学生根据校专业选考科目要求,结合自身特长兴趣,首先在物理、历史2门科目中选择 1门,再从思想政治、地理、化学、生物4门科目中选择1门参加考试。以文理科分开进行分数分值解释:
文科生:语文160分+40分(附加)、数学160分、英语120分、选修历史(必选)100分、选修X(自选)100分。
理科生:语文160分、数学160分+40分(附加)、英语120分、选修物理(必选)100分、选修X(自选)100分。
扩展资料2019年4月23日,江苏省人民政府召开“深化普通高校考试招生制度综合改革实施方案”新闻发布会,正式发布江苏2021年高考改革方案。实行“3+1+2”、不分文理、总分750分、使用全国卷模式。
选择性考试科目思想政治、历史、地理、物理、化学、生物6门。学生根据高校的要求结合自身特长兴趣首先在物理、历史2门科目中选择1门再从思想政治、地理、化学、生物4门科目中选择2门考试成绩计入考生总分作为统一高考招生录取的依据。
参加统一高考的学生可以用统一高考的语文、数学、外语科目考试替代相应科目的合格性考试。
百度百科-普通高等学校招生全国统一考试
百度百科-江苏高考新方案
中2013年江苏高考化学题第15题不明白,盼您详细讲解分析,谢谢! 正确答案为CD
2016江苏省高考化学
考试试卷
可能用到的相对原子质量:C-12 N-14 O-16 Mg-24 Si-28 S-32 Cl-35.5 Ca-40
选择题(共40分)
单项选择题:本题包括10小题,每小题2分,共计20分。每小题只有一个选项符合题意。
1.国务院颁布的《“十二五”控制温室气体排放工作方案》提出,2015年我国单位国内生产总值CO2排放要比2010年下降17%。下列说法不正确的是
A.CO2属于酸性氧化物 B.CO2是导致酸雨发生的主要原因
C.可用Na2CO3溶液捕捉(吸收)CO2 D.使用氢能源替代化石燃料可减少CO2排放
2.下列有关化学用语表示正确的是
A.过氧化钙(CaO2)的电子式:
B.8O离子的结构示意图:
+162- 2- C.H2CO3的电离方程式:H2CO3 2H+CO3
D.葡萄糖的结构简式:C6H12O6
3.常温下,下列各组离子在指定溶液中一定能大量共存的是
3+2- -- A.滴加石蕊试液显红色的溶液:Fe 、SO4、C1 、SCN
3++2- B.c(Al )=0.5mol·L 的溶液中:Na、K+、HCO3-、SO4
-+2-+-+ C.c(OH )/c(H)=10 的溶液中:SO3、NH4、NO3、K
+2+3+- D.滴加甲基橙试液呈红色的溶液:NH4、Ba 、Al 、Cl
4.下列物质性质与应用对应关系正确的是
A.硫酸铜溶于水呈酸性,可用来做杀菌剂
B.氨气具有还原性,可用于检查HCl泄漏
C.MgO、Al2O3熔点高,可用于制作耐高温坩埚
D.FeCl3溶液显酸性,可用于蚀刻印刷电路板
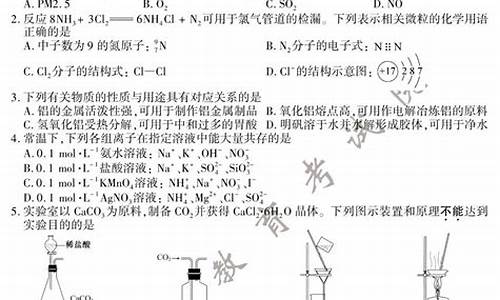
5.用下列实验装置进行相应实验,能达到实验目的的是
A.用图1装置作为制取少量二氧化硫的尾气吸收装置
B.用图2装置进行二氧化碳喷泉实验
C.用图3装置进行二氧化锰和浓盐酸制取氯气的实验
D.用图4装置进行石油的分馏实验
6.设NA为阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,2.24LCl2溶于足量水中转移电子的数目为0.1NA
B.标准状况下,22.4L苯中含有双键的数目为3NA
1/9页
C.常温下,16gO2和O3的混合气体中含有氧原子的数目为NA
+ D.25℃时,pH=1的醋酸溶液中含有H的数目为0.1NA
7.下列表示对应化学反应或过程的离子方程式正确的是
+2+ A.铜片插入硝酸银溶液中:Cu+Ag =Cu +Ag
2+-2-B.碳酸氢钙与过量的NaOH溶液反应:Ca+2HCO3+2OH-=CaCO3↓+2H2O+CO3
+- C.用稀硝酸除去试管内壁银:Ag+2H+NO3=Ag++NO2↑+H2O
+2- D.向氨水中通入过量SO2:SO2+2NH3?H2O=2NH4+SO3+H2O
8.已知甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下:
下列说法不正确的
A.若A为硝酸,X为金属元素,则甲与丙反应可生成乙
B.若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质
C.若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀
D.若乙为NaHCO3,则丙一定是CO2
9.下列依据相关实验得出的结论正确的是
A.向硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产 生,说明Ksp(BaCO3)<Ksp(BaSO4)
B.向淀粉溶液中加入稀硫酸并加热片刻,然后再加入适量银氨溶液进行水浴加热,没有 银镜生成,说明淀粉没有水解
C.将二氧化硫气体通入到高锰酸钾酸性溶液中,溶液紫红色褪去,说明二氧化硫有漂白性
D.向碳酸钠溶液中滴加几滴酚酞试液,然后再加入氯化钡溶液,溶液红色褪去,说明碳 酸钠溶液中存在水解平衡
10.短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,X与W同主族,Y、Z族序数之和为11,Z原子最外层电子数是内层电子总数的3倍。下列说法不.正确的是
A.元素Z、W的简单离子的电子层结构相同
B.元素Y的简单气态氢化物的热稳定性比Z的弱
C.W、Z两种元素形成的化合物中肯定不含共价键
D.由X、Y、Z三种元素形成的化合物,其水溶液可能显碱性
不定项选择题:本题包括5小题,每小题4分,共计20分。每小题只有一.个.或.两.个.选项符合题意。若正确答案只包括一个选项,多选时,该题得0分;若正确答案包括两个选项时,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就得0分。
11.下列说法正确的是
A.NaClO溶液中通入少量CO2,ClO-水解程度增大,溶液碱性增强
B.铁片镀锌时,铁片与外电源的正极相连
C.常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)能自发进行,则ΔH<0
D.t℃时,恒容密闭容器中反应:NO2(g
江苏化学高考是什么卷
分析:
A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同;
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动;
D.温度相同时,容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动.
解答:
解:
A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同,无法比较反应速率,故A错误;
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小,故B错误;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,故容器Ⅰ中CO 的物质的量比容器Ⅱ中的多,故C正确;
D.温度相同时,容器I中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,二氧化碳的转化率比两容器相同温度时容器Ⅱ中CO2的转化率低,故容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和小于1,故D正确.
故选CD.
2012江苏化学高考卷15题解析
截止至2023年11月21日,该考卷是新课标1卷。
江苏省的高考化学试卷是由江苏省自主命题的。因为在新的高考改革下,各省市可以自主命题选考科目。江苏省的高考模式是“3+1+2”,考生可以从物理、思想政治、地理等科目中选择一门首选科目和两门次选科目。江苏省的高考化学试卷是由江苏省自主命题的。
25°C时,有c(CH3COOH)+c(CH3COO-)=?0.?1?mol·L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH?的关系如图7?所示。下列有关溶液中离子浓度关系的叙述正确的是
A.?pH=5.?5?的溶液中:?c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B.?W?点所表示的溶液中:?c(Na+)+c(H+)=?c(CH3COOH)+c(OH-)
C.?pH?=?3.?5?的溶液中:c(Na+)?+c(H+)?-c(OH-)?+c(CH3COOH)=?0.?1mol·L-1
D.向W?点所表示的1.?0?L?溶液中通入0.?05?mol?HCl?气体(溶液体积变化可忽略):?c(H+)=?c(CH3COOH)+c(OH-)解释:物料守恒? c(CH3COOH)+c(CH3COO-)=?0.?1?mol·L-1=2c(Na+)
? 电荷守恒? c(Na+)+c(H+)=?c(CH3COO-)+c(OH-)
A.?pH=5.?5?的溶液中:c(H+)>c(OH-) 根据电荷守恒? c(CH3COO-)? >?c(Na+)
所以根据物料守恒?c(Na+)>?c(CH3COOH)? A错
B.?W?点所表示的溶液中:c(CH3COOH)? =?c(CH3COO-)?电荷守恒? c(Na+)+c(H+)=?c(CH3COO-)+c(OH-)
所以 c(Na+)+c(H+)=?c(CH3COOH)+c(OH-) 正确
C?
物料守恒? c(CH3COOH)+c(CH3COO-)=?0.?1?mol·L-1
? 电荷守恒? c(Na+)+c(H+)=?c(CH3COO-)+c(OH-)?
合并推导C 正确
D 溶液中多0.05molHCl
物料守恒? c(CH3COOH)+c(CH3COO-)=?0.?1?mol·L-1=2c(Na+)
? 电荷守恒? c(Na+)+c(H+)=?c(CH3COO-)+c(OH-)+c(Cl—)
合并推导得
2c(H+)+c(CH3COOH)=?c(CH3COO-)+2c(OH-)+2C(Cl—)
D?错









