您现在的位置是: 首页 > 教育分析 教育分析
碘和钾高考题-高碘酸钾中碘的化合价
tamoadmin 2024-08-22 人已围观
简介1.碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).图是超市销售的一种加碘盐标签上2.碘 碘酸钾 碘化钾 化学问题 求解释3.碘酸钾(KIO 3 )晶体是我国规定的食盐加碘剂。它通常是以碘为原料与过量KOH溶液通过下列反应制得:3I 24.碘和钾反应方程式碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).图是超市销售的一种加碘盐标签上(1)根据碘酸钾的
1.碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).图是超市销售的一种加碘盐标签上
2.碘 碘酸钾 碘化钾 化学问题 求解释
3.碘酸钾(KIO 3 )晶体是我国规定的食盐加碘剂。它通常是以碘为原料与过量KOH溶液通过下列反应制得:3I 2
4.碘和钾反应方程式
碘元素对青少年智力发育影响很大,加碘盐通常在食盐中加碘酸钾(KIO3).图是超市销售的一种加碘盐标签上
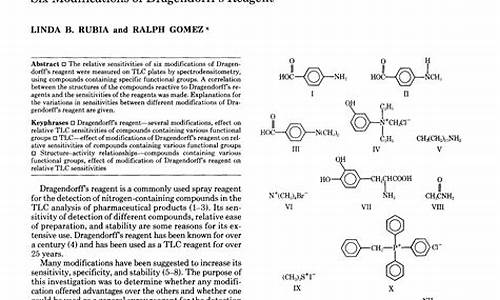
(1)根据碘酸钾的化学式(KIO3)可知,碘酸钾(KIO3)中钾、碘、氧三种元素原子个数比为1:1:3;碘酸钾中钾、碘、氧三种元素质量比=(39×1):(127×1):(16×3)=39:127:48;
(2)碘酸钾中碘元素的质量分数=
| 127 |
| 214 |
(3)每袋该食盐中碘元素的质量=0.5kg×20mg∕kg=10mg;
(4)根据题中信息“勿长时间加热”可推出碘酸钾受热易分解;
故答案为:
(1)1:1:3;39:127:48;
(2)59.3%;
(3)10;
(4)受热易分解.
碘 碘酸钾 碘化钾 化学问题 求解释
一式是氧气把碘离子氧化成碘单质,和后两个应该不同类的
二式和三式:
首先他俩不算可逆反应,反应条件不同。
二式碱性环境下反应,三式酸性。因此做题时不难区分,只要看溶液酸碱性就可以了。
其实就是碘加碱歧化,加酸归中。
碘酸钾(KIO 3 )晶体是我国规定的食盐加碘剂。它通常是以碘为原料与过量KOH溶液通过下列反应制得:3I 2
| (1)5:1 (2)I - +6OH - -6e - =IO 3 - +3H 2 O氢气 (3)IO 3 - + 5I - +6H + =3I 2 +3H 2 O 实验操作取少量阳极区电解液于试管中,加稀硫酸酸化后,加入几滴淀粉 溶液,观察是否变蓝 现象及结论如果不变蓝,说明没有I - (如果变蓝,说明有I - ) (4)蒸发浓缩,洗去吸附在碘酸钾晶体表面的氢氧化钾等杂质 |
| 试题分析:(1)碘元素由0价升为+5价,则I 2 是还原剂,KIO 3 是氧化产物,碘元素还由0价降为—1价,则I 2 还是氧化剂,KI是还原产物;根据系数之比等于物质的量之比,由于氧化产物KIO 3 为1mol,则还原剂I 2 为1/2mol,还原产物KI为5mol,则氧化剂I 2 为5/2mol,所以该反应中氧化剂和还原剂的物质的量之比为5/2∶1/2=5∶1;(2)阳极发生氧化反应,根据题意可知其主要反应物和产物是I ― →IO 3 ― ;碘元素由—1价升为+5价,根据化合价升高总数等于失去电子数可知,I ― —6e ― →IO 3 ― ;根据KOH溶液显碱性可知,应用OH ― 使左右电荷守恒,则I ― —6e ― +6OH ― →IO 3 ― ;根据氢或氧原子个数守恒可知,I ― —6e ― +6OH ― =IO 3 ― +3H 2 O;溶液中的阳离子移向阴极,H + 优先得到电子,发生还原反应,产生氢气,则阴极得到的气体产物是H 2 ;(3)碘元素由+5价降为0价,说明KIO 3 是氧化剂,I 2 是还原产物,碘元素由—1价升为0价,说明I ― 是还原剂,I 2 还是氧化产物;根据化合价升降总数相等,则IO 3 ― +5I ― →3I 2 ;酸性介质中可用H + 使左右电荷守恒,则IO 3 ― +5I ― +6H + →3I 2 ;根据氢或氧原子守恒可知,该反应为IO 3 ― +5I ― +6H + =3I 2 +3H 2 O;检验阳极区电解液中I ― 时,需要借助上述反应中碘离子的氧化产物(碘单质)遇淀粉变蓝的特性,就是要设法使碘离子转化为碘单质;因此实验时先取少量阳极区电解液于试管中,加稀硫酸酸化后,再加入几滴淀粉溶液,观察是否变蓝,若不变蓝,说明无碘离子;若变蓝,说明有碘离子;(4)根据混合物分离提纯的方法可知,从KIO 3 溶液中制KIO 3 晶体的过程分别为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则步骤①为蒸发浓缩;KIO 3 晶体上吸附着KOH等易溶性杂质,洗涤的目的是除去晶体表面吸附的易溶性杂质。 |
碘和钾反应方程式
2KIO3=(加热)2KI+3O2(气)。化学方程式: 2KIO3=(加热)2KI+3O2(气) 碘酸钾即KIO3,受热分解反应方程式是:碘酸钾在加热的条件下生成碘化钾和氧气,具体化学方程式是:2KIO3=(加热)2KI+3O2(气),碘酸钾,是一种无机化合物,化学式为KIO3,分子量为214.001,为白色结晶性粉末。溶于水、稀硫酸,溶于碘化钾溶液,不溶于乙醇、液氨。由硝酸氧化单质碘得到碘酸,再用氢氧化钾中和或将碘化钾的碱性溶液电解氧化而得。
上一篇:高考微博励志-高考微博文案









